Вы используете устаревший браузер. Этот и другие сайты могут отображаться в нём некорректно.
Вам необходимо обновить браузер или попробовать использовать другой.
Вам необходимо обновить браузер или попробовать использовать другой.
-
Премедикация. Подготовка больного к операции
30 Сен 2017 - Хирургия
-
Биохимия витаминов
24 Сен 2017 - Биохимия
Фильтры
Показывать только:
Загрузка...
-
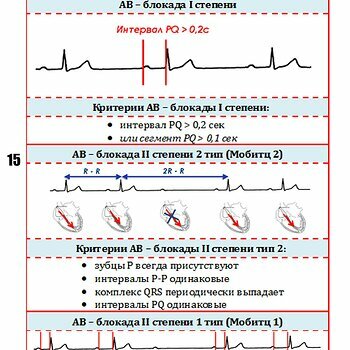
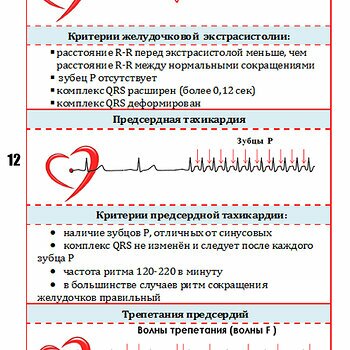
Острая ревматическая лихорадка и хроническая ревматическая болезнь сердца
Острая ревматическая лихорадка (ОРЛ) – системное воспалительное заболевание соединительной ткани, возникающее у предрасположенных лиц, после...-
1 Мар 2020 - 2K
- 1
- Ревматология
-
-
Методика работы на синоптофоре
Введение В последние годы при диагностике и лечении косоглазия все большее применение находят синотипные приборы. Преимущество их состоит в... -
Хирургические инструменты
Классификация хирургических инструментов Операция включает ряд последовательных этапов: рассечение тканей, их разведение, фиксацию, оперативный...-
23 Ноя 2019 - 57K
- Хирургия
-
-
Диагностические критерии ревматоидного артрита
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ РЕВМАТОИДНОГО АРТРИТА 1987 (пересмотренные. Американская ревматологическая ассоциация, 1987 г.) 1. Утренняя скованность... -
Экспертиза временной нетрудоспособности
Экспертиза временной нетрудоспособности – это вид медицинской деятельности, основной целью которой является оценка состояния здоровья пациента... -
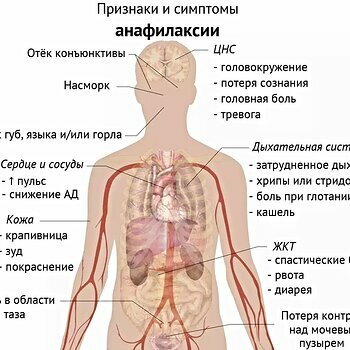
Неотложная помощь. Анафилактический шок
Этиология Возникает в первые минуты после поступления в организм аллергена: Лекарственные средства (антибиотики, нестероидные... -
Ранняя диагностика меланомы (АККОРД-меланома)
Родинки есть у подавляющего большинства людей, но предрасположенность к развитию атипичных родинок в ряде случаев является наследственной. Если... -
Общие вопросы экспертизы трудоспособности
Врачебная экспертиза трудоспособности является важнейшей сферой практической деятельности в здравоохранении, которая тесно соприкасается с... -
Дефицитные состояния у детей раннего возраста: рахит и недостаточность витамина D
«ДЕФИЦИТНЫЕ СОСТОЯНИЯ У ДЕТЕЙ РАННЕГО ВОЗРАСТА: РАХИТ И НЕДОСТАТОЧНОСТЬ ВИТАМИНА Д» Рахит – заболевание растущего организма. Чем меньше ребенок... -
Ревматоидный артрит: патогенез, клиника, диагностика, лечение
Ревматоидный артрит Ревматоидный артрит (РА) — хроническое воспалительное заболевание неизвестной этиологии, характеризующееся симметричным... -
Физиологические роды. Первый период родов
Физиологические роды. Первый период родов Средняя продолжительность физиологических родов составляет 7–12 (до 18) часов. Роды, продолжающиеся... -
Партограмма нормальных родов
Перед началом родов шейка размягчена, что обеспечивает более легкое ее раскрытие. Если эти подготовительные изменения недостаточны, то... -
Гормоны: характеристика, свойства и влияние на физиологические процессы
Введение Все ткани животного организма обладают внутри секреторной или эндокринной функцией. В процессе жизнедеятельности они образуют...-
28 Фев 2018 - 2K
- 1
- Физиология
-
-
Нейрон: структурно-функциональная единица нервной системы
Введение Нейрон - (от греч. neuron — нерв), неврон, нервная клетка, основная функциональная и структурная единица нервной системы, принимает... -
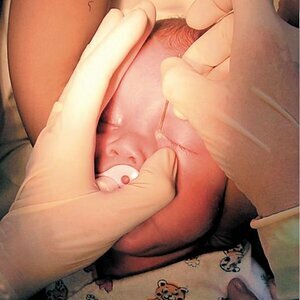
Признаки отделения и приемы выделения плаценты
Признаки отделения плаценты Признак Шредера – изменение формы и высоты стояния дна матки. Сразу после рождения плода матка принимает округлую... -
Премедикация. Подготовка больного к операции
Подготовка больного к операции Перед любой анестезией, выполняемой в плановом порядке, необходимо: побеседовать с больным о предстоящей...-
30 Сен 2017 - 63K
- 1
- Хирургия
-
-
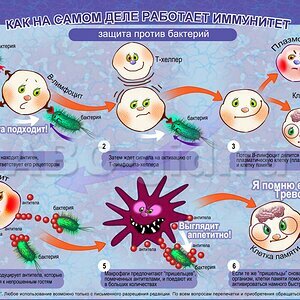
Органы кроветворения и иммунной системы
Красный костный мозг Красный костный мозг - является главным органом кроветворения и одновременно органом иммунной системы. У новорождённых он... -
Анатомия желудка
Анатомия желудка В желудке различают кардиальный отдел, субкардию, дно, тело и антральный отдел. 1). Кардиальный отдел - часть желудка... -
Определение срока беременности и даты родов
Определение срока беременности производят на основании анамнестических данных, по результатам объективного обследования: По дате последней... -
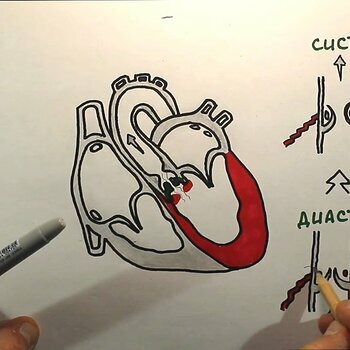
Строение сердца
Сердце Топография сердца: 1. Верхняя граница проходит по линии соединяющей верхние края хрящей правого и левого третьих ребер. 2. Правая граница...
Категории
Пользователи онлайн
Сейчас на форуме нет ни одного пользователя.
Всего: 1 (пользователей: 0, гостей: 1)
Сообщения профилей
Быть энергичным, хорошо себя чувствовать, жить полноценной жизнью до глубокой старости, прожить как можно дольше – менее чем на 20% зависит от генов, а более чем на 50% от образа жизни, который вы выбираете сами.
Статистика статей
- Категории
- 12
- Статьи
- 33
- Серии
- 2
- Просмотры
- 348,776
- Комментарии
- 1
- Оценки
- 0
- Отзывы
- 0
Статистика форума
Облако тегов
eksmo анатомия атлас биостатистика вебер доказательная медицина за 3 дня кардиология книги о тех кто спасает жизни конспект лекций краткое издание медицина без границ методичка наглядная медицина национальное руководство неотложка полный курс за 3 дня руководство схемы вебера таблицы учебное пособие экзамен в кармане